衰老是心血管疾病的重要风险因素。随着我国人口老龄化的加剧,衰老相关的心血管疾病已经成为导致城乡居民死亡的首位原因。不过,有大量证据显示,可以通过调控衰老相关的信号通路来改善血管健康,从而促进生命健康并延长寿命。因此,通过促进血管“再年轻化(Rejuvenation)”来抵抗衰老和相关疾病的发生,是一个新颖、可行的研究思路。
近日,中国医学科学院相关研究团队在European Heart Journal(39.3)杂志发表了相关文章[1],将国自然三大热点“衰老、血管重塑和氧化应激”结合起来,首次证明了作为一种表观遗传调节因子,SIRT2可以通过细胞质-线粒体穿梭机制调控血管衰老,为破解血管衰老之谜提供了重要的参考依据。

一、研究内容与思路
1、SIRT2在人和小鼠血管老化中的表达和活性
为了测试Sirtuins在血管老化中的潜在作用,作者分析了人和小鼠主动脉中SIRT1-SIRT7 mRNA的基础水平,发现SIRT2在人与小鼠主动脉中的基础表达水平最高。
因此,作者测试了年轻和老年小鼠主动脉中SIRT2的酶活性以及蛋白表达水平,发现:相比于年轻小鼠,老年小鼠主动脉中SIRT2活性及蛋白表达水平均显著降低。
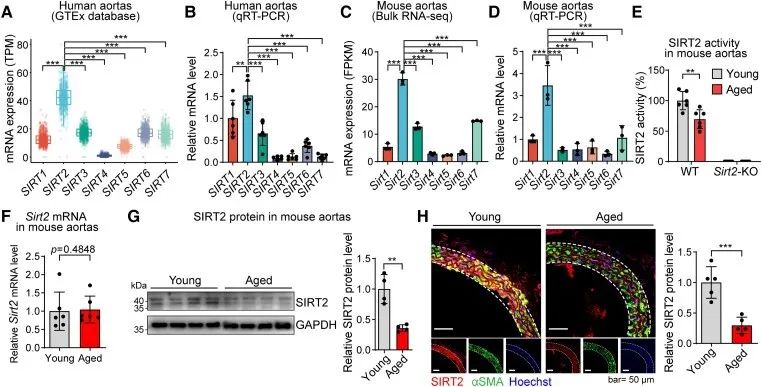
研究思路:作者首先明确研究目标—Sirtuins家族,之后根据分析结果锁定到SIRT2,并将其作为研究主角。
2、SIRT2缺乏促进衰老诱导的血管功能障碍和重塑
接下来,作者评估了SIRT2对衰老诱导的血管功能障碍的影响。测量了脉搏波速度(PWV)和动脉收缩-舒张功能之后,发现与年轻小鼠相比,老年小鼠的PWV值显著升高,且主动脉血管收缩受到损害,而在SIRT2敲低的老年小鼠中,这些情况进一步恶化,表明SIRT2缺失会加剧衰老引起的血管功能障碍。
作者采用解剖学和组织学分析以测试老年SIRT2沉默小鼠血管功能障碍出现恶化是否与血管重塑有关,结果发现:老年SIRT2沉默小鼠主动脉重量与体重(AW/BW)比率增加,对于血管重塑和衰老至关重要的MMP2和MMP9过度表达。以上结果表明,SIRT2可能调节MMP参与的年龄依赖性血管重塑和僵化。
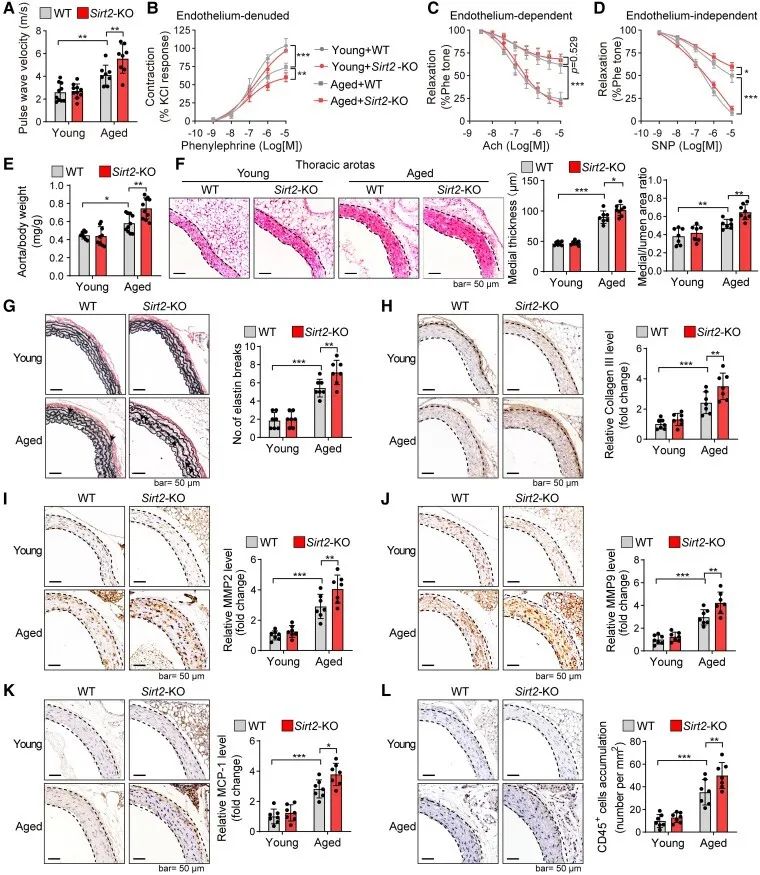
研究思路:SIRT2在衰老小鼠主动脉高表达,那对于年龄依赖性血管重塑起到什么作用?以及是如何发挥作用的?
3、SIRT2缺乏会重编程血管转录组并加重线粒体氧化应激
为了进一步阐明SIRT2在年龄依赖性血管重塑和僵化中的作用机制,作者分析了小鼠衰老主动脉转录组测序结果,发现老龄小鼠在SIRT2缺失后,主动脉中与年龄依赖性动脉疾病相关的基因集富集,此外,SIRT2的缺失导致氧化应激相关基因的富集。以上表明,SIRT2可能通过调节氧化应激来影响年龄依赖性动脉疾病。对此,作者开展了验证,发现敲除SIRT2增加了衰老诱导的小鼠主动脉中总超氧化物(DHE)和线粒体超氧化物(mROS)的上调,而给予氧化应激诱导剂血管紧张素II(Ang II)和特异性Sirt2抑制剂AGK2也可以得到以上结论。
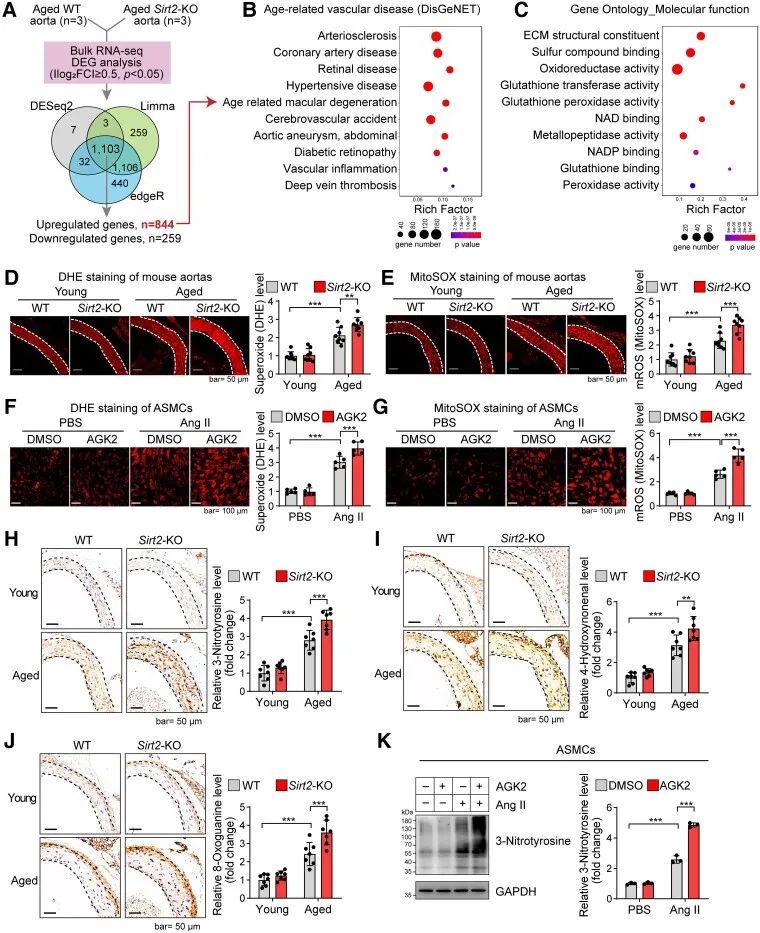
研究思路:明确了SIRT2对于年龄依赖性血管重塑的作用后,作者进一步采用测序来探究其富集基因及通路,并开展验证,发现SIRT2缺乏会导致血管转录组重编程以及加重线粒体氧化应激。
4、SIRT2抑制p66SHc靶向线粒体活性氧积累
因为SIRT2调节组蛋白和非组蛋白的赖氨酸修饰,对此,作者检测了SIRT2是否是通过组蛋白修饰来直接调节血管转录组,结果发现SIRT2是间接调节血管转录的。作者将目光转移到与氧化还原相关并且是已知的衰老因子的蛋白p66Shc身上,蛋白p66Shc通过调节氧化还原相关基因的转录来影响衰老诱导的血管重塑和寿命。作者发现SIRT2显著上调p66Shc磷酸化,促进p66Shc线粒体的易位和氧化应激(mROS)。
在主动脉平滑肌细胞(ASMC)中,过表达SIRT2会抑制p66Shc的磷酸化以及乙酰化,进一步发现p66Shc在SIRT2调节血管细胞中的氧化应激和MMP中也发挥着作用。综上所述:SIRT2沉默会刺激p66Shc表达并刺激线粒体氧化应激以及血管转录组重编程,从而加速衰老诱导的血管重塑。
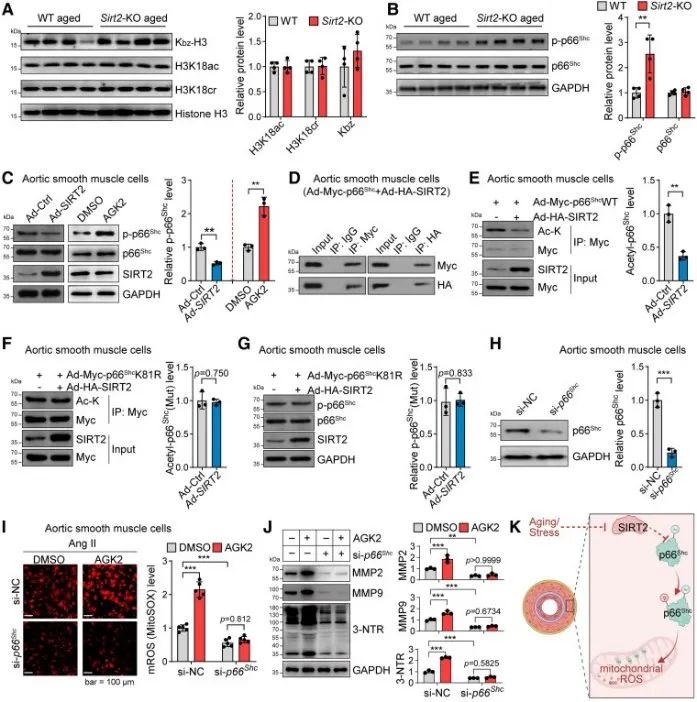
研究思路:那SIRT2是直接通过氧化应激来发挥作用嘛?还是中间存在着其他因子发挥作用,对此,作者首先实验排除了直接发挥作用,之后将目光锁定在与氧化还原相关并且是已知的衰老因子,结合课题组研究内容,最终锁定p66SHc并开展验证。
5、ROS有助于血管老化中的SIRT2功能
作者探索了ROS在SIRT2缺陷介导的血管重塑中的作用,发现SIRT2缺乏促进了小鼠DHE和mROS的积累和大分子氧化,诱导了血管功能障碍,包括血管硬度降低和收缩-舒张功能障碍。
进一步,作者采用超氧化物歧化酶模拟物和超氧化物清除剂Mn TBAP注射治疗老龄小鼠及SIRT2缺陷老龄小鼠,结果发现Mn TBAP治疗挽救了SIRT2缺乏导致的ROS积累及大分子氧化,抑制小鼠血管功能障碍,阻断SIRT2缺乏对衰老诱导的血管功能障碍的影响,显著增加血管硬度,改善血管收缩-松弛功能障碍。
这些发现表明,ROS有助于血管重塑中的SIRT2功能,并可能作为治疗已确诊血管老化的靶点。
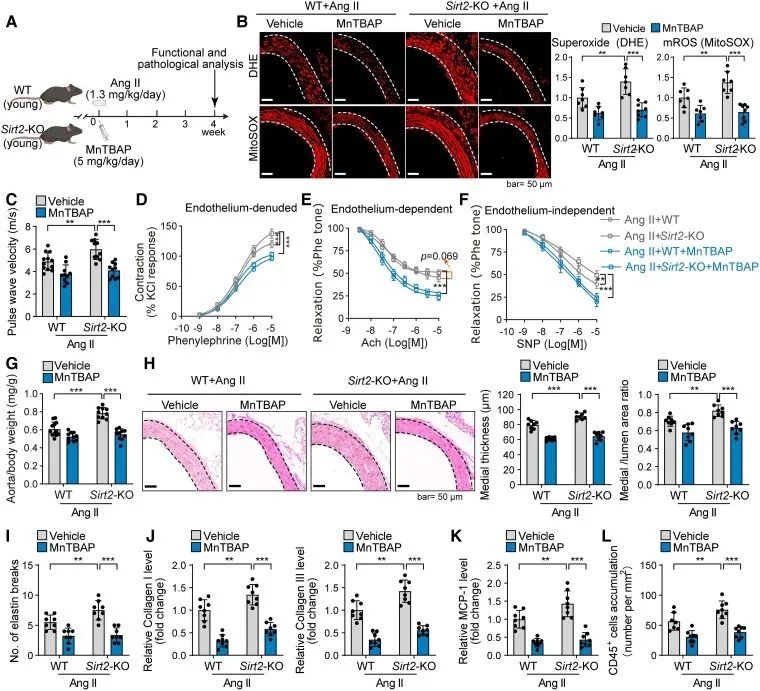
研究思路:明确了ROS是发挥作用的最后一环后,作者进一步探索ROS能不能反作用于SIRT2,从而形成互相影响作用以及闭环。
6、SIRT2与人类衰老相关的血管重塑和相关疾病有关
为了探索SIRT2在人类血管衰老中的潜在意义,作者使用公共蛋白质组数据集、人和小鼠SIRT2共表达网络分析(WGCNA)检测人类整个生命周期的血浆SIRT2水平。发现血浆中SIRT2水平与年龄呈负相关,而这一环节可能与氧化还原系统和线粒体代谢相关,SIRT2共表达模块对腹主动脉瘤(AAA)和主动脉闭塞性疾病(AOD)具有预测意义。这些发现表明,SIRT2共表达模块对衰老和与年龄相关的主动脉疾病具有预测意义。
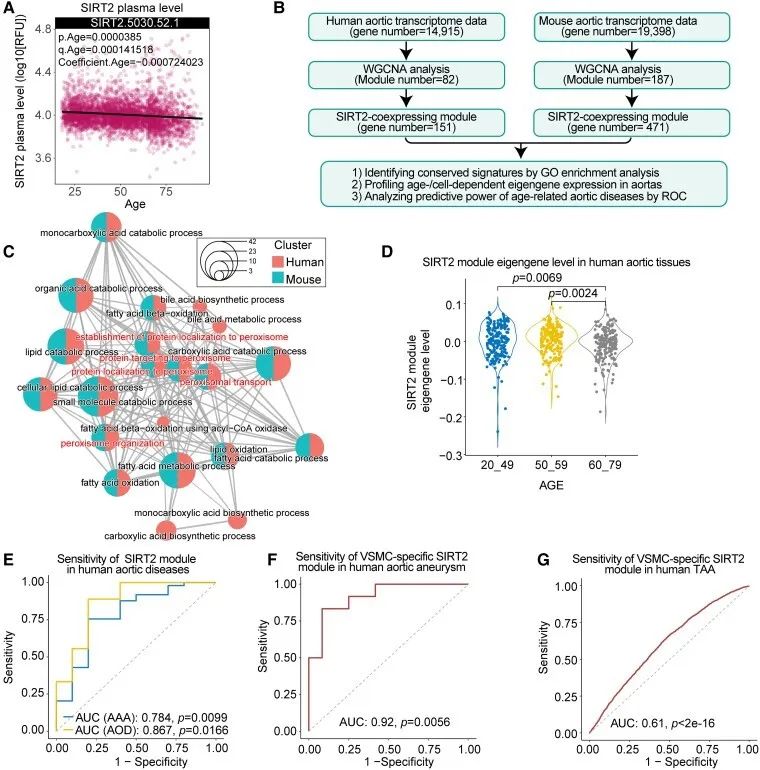
研究思路:将整个作用环节以及机制明确后,作者重新回归临床及显示,将所得结果与人群数据结合,从而表明所得结果在人群中也是适用的,并且可以作为衰老相关血管疾病的潜在治疗靶点。
二、小结
作者首先在人类和小鼠主动脉检测到SIRT2的高表达;之后通过一系列动物实验发现SIRT2会进一步加剧血管功能障碍,参与年龄依赖性血管重构等;进一步探索其机制,发现SIRT2-p66shc–mROS轴对血管转录组进行重编程,参与了衰老小鼠的血管重塑与功能障碍;最后回归人群中,证实SIRT2失调与人类血管老化和疾病有关,是衰老相关血管疾病的潜在治疗靶点。
这一研究思路环环相扣,最后将实验所得结果与实际相结合,拔高研究深度。
参考文献:
[1] Zhang, Yang et al. “Sirtuin 2 deficiency aggravates ageing-induced vascular remodelling in humans and mice.” European heart journal vol. 44,29 (2023): 2746-2759. doi:10.1093/eurheartj/ehad381













